ظرفیت یک عنصر معیاری از ظرفیت ترکیب شوندگی آن است و می توان آن را به این صورت تعریف کرد:
تعداد الکترون هایی که باید توسط یک اتم از دست داده یا به دست آید تا یک پیکربندی الکترونی پایدار به دست آید.
اصطلاح “عدد اکسایش” به چه معناست؟
عدد اکسایش یک اتم بیانگر تعداد الکترون های از دست رفته یا به دست آمده توسط اتم است.
عدد اکسایش و ظرفیت یکی از اساسی ترین ویژگی های عناصر است و می توان آن را با کمک آرایش های الکترونی بررسی کرد.
ظرفیت و عدد اکسایش
الکترون هایی که در بیرونی ترین پوسته یافت می شوند عموماً به عنوان الکترون های ظرفیت شناخته می شوند و تعداد الکترون های ظرفیت ،تعیین کننده ظرفیت یک اتم است.
ظرفیت عناصر متعلق به ستون s و ستون p جدول تناوبی به طور کلی به صورت تعداد الکترون ظرفیت یا هشت منهای تعداد الکترون های ظرفیت محاسبه می شود.
برای عناصرستون dو ستونf ظرفیت نه تنها بر اساس الکترون های ظرفیت بلکه بر روی الکترون های مداری d و f نیز تعیین می شود. با این حال، ظرفیت کلی عناصرستونf, d 2 و3است.
حالت کلی اکسیداسیون عناصر جدول تناوبی در نمودار زیر نشان داده شده است.
نمودار عدد اکسایش و ظرفیت
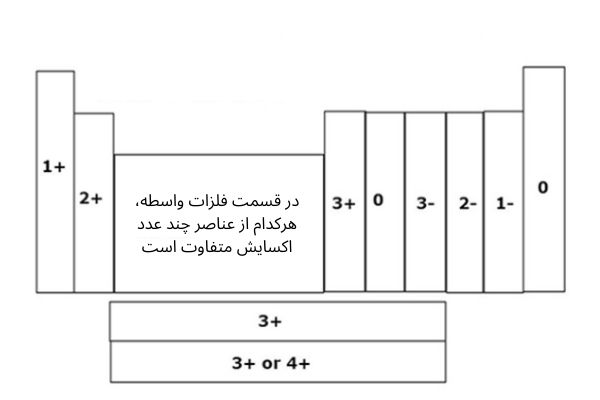
ظرفیت 30 عنصر اول
ظرفیت 30 عنصر اول جدول تناوبی در زیر آورده شده است.
| عنصر | شماره اتمی | ظرفیت |
| ظرفیت هیدروژن | 1 | 1 |
| ظرفیت هلیوم | 2 | 0 |
| ظرفیت لیتیوم | 3 | 1 |
| ظرفیت بریلیم | 4 | 2 |
| ظرفیت بور | 5 | 3 |
| ظرفیت کربن | 6 | 4 |
| ظرفیت نیتروژن | 7 | 3 |
| ظرفیت اکسیژن | 8 | 2 |
| ظرفیت فلوئور | 9 | 1 |
| ظرفیت نئون | 10 | 0 |
| ظرفیت سدیم (Na) | 11 | 1 |
| ظرفیت منیزیم (Mg) | 12 | 2 |
| ظرفیت آلومینیوم | 13 | 3 |
| ظرفیت سیلیکون | 14 | 4 |
| ظرفیت فسفر | 15 | 3 |
| ظرفیت گوگرد | 16 | 2 |
| ظرفیت کلر | 17 | 1 |
| ظرفیت آرگون | 18 | 0 |
| ظرفیت پتاسیم (K) | 19 | 1 |
| ظرفیت کلسیم | 20 | 2 |
| ظرفیت اسکاندیم | 21 | 3 |
| ظرفیت تیتانیوم | 22 | 4 |
| ظرفیت وانادیوم | 23 | 5,4 |
| ظرفیت کروم | 24 | 2 |
| ظرفیت منگنز | 25 | 7, 4, 2 |
| ظرفیت آهن (آهن) | 26 | 2, 3 |
| ظرفیت کبالت | 27 | 3, 2 |
| ظرفیت نیکل | 28 | 2 |
| ظرفیت مس | 29 | 2, 1 |
| ظرفیت روی | 30 | 2 |
بقیه عناصر شیمیایی جدول تناوبی را میتوانید در اینجا مشاهده کنید.
روندهای دوره ای در عدد اکسایش عناصر
-
تغییر عدد اکسایش در طول یک دوره
در حین حرکت از چپ به راست در طول یک دوره، تعداد الکترون های ظرفیت عناصر افزایش می یابد و بین 1 تا 8 تغییر می کند. اما ظرفیت عناصر، وقتی ابتدا با H یا O ترکیب می شود، از 1 به 4 افزایش می یابد و سپس به صفر کاهش می یابد. دو ترکیب حاوی اکسیژن Na2O و F2O را در نظر بگیرید.
در F2O، الکترونگاتیوی F بیشتر از اکسیژن است. بنابراین، هر یک از اتم های F یک الکترون از اکسیژن جذب می کند، یعنی F عدد اکسایش -1 و O عدداکسایش +2 را نشان می دهد. در حالی که در مورد Na2O، اکسیژن نسبت به اتم سدیم بسیار الکترونگاتیو است. بنابراین اکسیژن از هر اتم سدیم دو الکترون را جذب می کند که حالت اکسیداسیون -2 را نشان می دهد و Na حالت اکسیداسیون +1 خواهد داشت. حالت اکسیداسیون عنصر نشان دهنده باری است که یک اتم به دلیل از دست دادن یا افزایش الکترون ها (به دلیل اختلاف الکترونگاتیوی بین اتم های ترکیب شده) در مولکول دارد.
-
تغییر حالت اکسیداسیون در یک گروه
همانطور که در یک گروه به سمت پایین حرکت می کنیم، تعداد الکترون های ظرفیت تغییر نمی کند. از این رو، تمام عناصر یک گروه دارای ظرفیت یکسانی هستند.
روش هایی برای تعیین عدد اکسایش
عدد اکسایش عناصری مانند O2، S8، H2، P4، Fe و غیره صفر است.
اکسیژن عدد اکسایش 2- دارد. اما در پراکسیدهایش مانند Na2O2 و H2O2 عدد اکسایش -1 دارد
به طور مشابه، هیدروژن عدد اکسایش 1+ دارد. اما در متال هیدریدها مانند NaH، LiH و غیره دارای عدد اکسایش -1 است
برخی از عناصر همان عدد اکسایشی را دارند که در ترکیبات آنها وجود دارد مانند
هالوژن ها عدد اکسایش 1- دارند به جز زمانی که با یکدیگر یا با اکسیژن ترکیب میشوند.
فلزات قلیایی مانند Na، K، Rb، Li،Cs دارای عدد اکسایش 1+ میباشد
فلزات قلیایی خاکی دارای عدد اکسایش+2 هستند مانند Mg، Ca، Ba، Be، Sr و غیره


مشاوره آنلاین از چه طریقی صورت می گیره؟
چه مطلب خوبی
مطالب بی نظیر بود
سلام عالی بود
قیمت مشاورتون چقدره؟
خیلی عالی بود
دمتون گرم
بیشتری بنویسین لطفا
مطلب خوبی بود همکار گرامی
خیلی خوشحالم که هستین
منابع این مطلب کجاست؟