واکنش تجزیه چیست؟
واکنش تجزیه را می توان به عنوان یک واکنش شیمیایی تعریف کرد که در آن یک واکنش دهنده به دو یا چند محصول تجزیه می شود.
فرمت واکنش عمومی
فرمت کلی واکنش تجزیه در زیر ارائه شده است.
AB -> A + B
جایی که AB مولکول اصلی (واکنش دهنده) و A & B مولکول های محصول هستند.
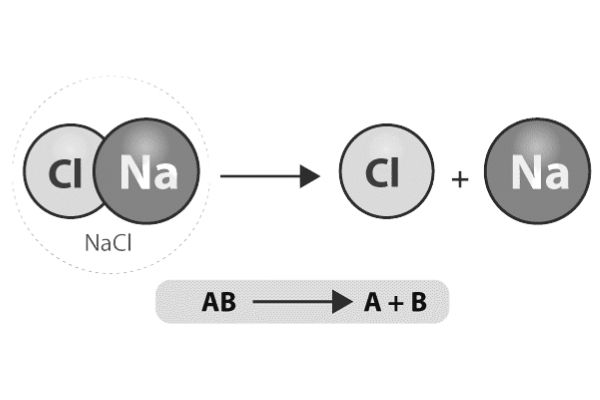
واکنش تجزیه
نمونه های واکنش تجزیه
واکنش های تجزیه در اطراف ما اتفاق می افتد، اما ما اغلب متوجه آنها نمی شویم. چند نمونه متداول از واکنش های تجزیه در زیر ارائه شده است.
- تجزیه کربنیک اسید در نوشابه ها که می توان آن را با معادله شیمیایی H2CO3 → H2O + CO2 نشان داد.
- الکترولیز آب برای تولید هیدروژن و اکسیژن.
مخالف “واکنش تجزیه” چیست؟
نقطه مقابل واکنش تجزیه یک واکنش ترکیبی است. چنین واکنش هایی شامل تشکیل یک محصول واحد از دو یا چند واکنش دهنده است.
آیا همه واکنش های تجزیه گرماگیر هستند؟
خیر، همه واکنش های تجزیه گرماگیر نیستند. یک واکنش تجزیه می تواند هم گرماگیر یا هم گرمازا باشد. با این حال، دومی شایع تر از اولی است. مثلا:
- تجزیه NO به N2 و O2 گرمازا است.
- تجزیه ازن (O3) به اکسیژن (O2) گرمازا است.
کاربردهای واکنش های تجزیه چیست؟
یکی از کاربردهای عمده واکنش های تجزیه در استخراج فلزات از سنگ معدن آنها است. به عنوان مثال، روی را می توان از کالامین با قرار دادن آن در یک واکنش تجزیه به دستآورد. به روشی مشابه، سدیم را می توان از کلرید سدیم (NaCl) یا دیگر ترکیبات سدیم (برای مشاهده به https://echemicals.ir/product-category/sodium/ مراجعه کنید) به دستآورد.
واکنش تجزیه دوگانه
واکنش تجزیه مضاعف نوعی واکنش تجزیه است که در آن دو واکنش دهنده تشکیل دهنده، یون های مثبت و منفی را تعویض کرده و دو ترکیب جدید را تشکیل می دهند.
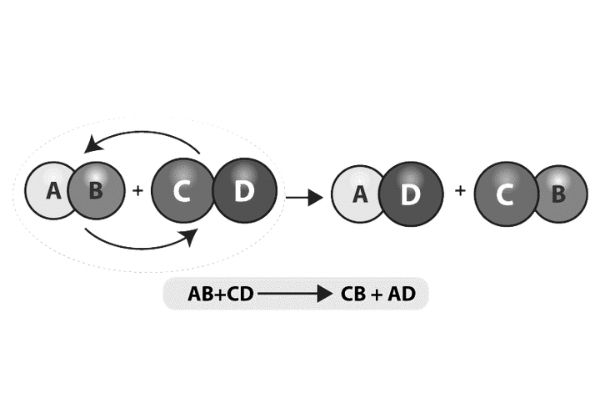
مثال:
HCl(aq) + NaOH(aq) → NaCl(aq) + HOH(l)
انواع واکنش تجزیه
سه نوع اولیه واکنش های تجزیه عبارتند از: حرارتی، الکترولیتی و فتوشیمیایی
در زیر هر سه مورد را به صورت کامل توضیح داده ایم.
واکنش تجزیه حرارتی
واکنش تجزیه حرارتی را می توان به عنوان یک واکنش تجزیه ای تعریف کرد که توسط انرژی حرارتی فعال می شود. به عبارت دیگر، یک واکنش تجزیه حرارتی نیاز به انرژی دارد تا به شکل گرما به واکنش دهنده ها برسد. چنین واکنش هایی عموما گرماگیر هستند؛ زیرا برای شکستن پیوندهای شیمیایی و جداسازی عناصر تشکیل دهنده به انرژی نیاز است. یک مثال معمول از واکنش تجزیه حرارتی در زیر ارائه شده است.
CaCO3 → CaO + CO2
کربنات کلسیم با حرارت دادن به اکسید کلسیم و دی اکسید کربن تجزیه می شود. این فرآیند در ساخت آهک زنده که یک ماده مهم در بسیاری از صنایع است، استفاده می شود.
برای تمرین فکر میکنید که کربنات پتاسیم با حرارت دادن به چه چیزی تبدیل میشود؟
واکنش تجزیه الکترولیتی
واکنش تجزیه الکترولیتی نوعی واکنش تجزیه است که در آن انرژی فعال سازی برای تجزیه به صورت انرژی الکتریکی تامین می شود. نمونه ای از واکنش تجزیه الکترولیتی، الکترولیز آب است که می توان آن را با معادله شیمیایی زیر نشان داد:
2H2O→ 2H2 + O2
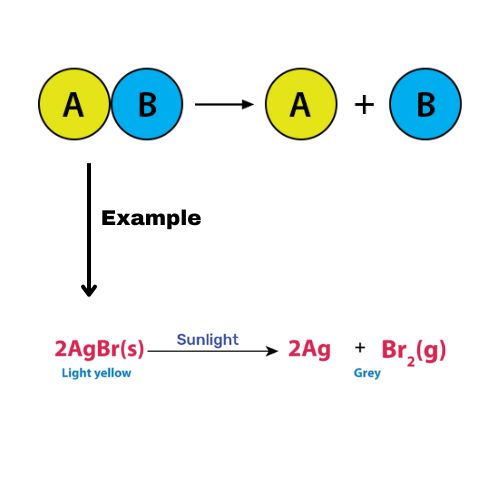
تجزیه عکس / تجزیه فوتولیتیک / تجزیه فتوشیمیایی
واکنش تجزیه نوری نوعی واکنش تجزیه است که در آن واکنش دهنده با جذب انرژی از فوتون ها به اجزای تشکیل دهنده خود تجزیه می شود. نمونهای از واکنش تجزیه عکس، تجزیه به دیاکسیژن و رادیکال اکسیژن است که با معادله شیمیایی ارائهشده در زیر نشان داده شده است.
O3 + hν → O2 + O
موارد استفاده از واکنش های تجزیه
- تولید سیمان یا اکسید کلسیم.
- برای فرآیندهای متالورژی: استخراج فلزات از اکسیدها، کلریدها و غیره آنها.
- تسکین سوء هاضمه اسیدی
- جوشکاری ترمیت.


چه مطلب خوبی
خیلی ممنون از توضیحاتون خوبتون
چرا اینقد زیاد؟
چجوری می تونیم با کارشناسانتون در ارتباط باشیم
مطلب به درد بخوری بود
من مشاوره برای رابطه می خواستم چجوری باهاتون ارتباط بر قرار کنم
هزینه مشاورتون چنده؟
aaaaliii bood
لطفا آدرستون رو برای بنده ارسال کنین دکان هم دارین
دفتر مرکزیتون کجا قرار داره
دمتون گرم